近日,天津医科大学肿瘤医院李悦国教授课题组在肝脏纤维化研究领域取得了突破性进展。相关成果以题为 “Hepatocyte-specific C-C motif chemokine ligand 9 signaling promotes liver fibrosis progression in mice” 的论文,于2025年5月在线发表于国际顶级肝病学期刊《Hepatology》(五年影响因子15.5)。本研究首次阐明肝细胞源性Ccl9通过双重机制驱动肝纤维化进程,而肝纤维化作为肝癌发生的关键前驱病变,该发现为肝癌高危人群的早期防治策略提供了潜在靶标。

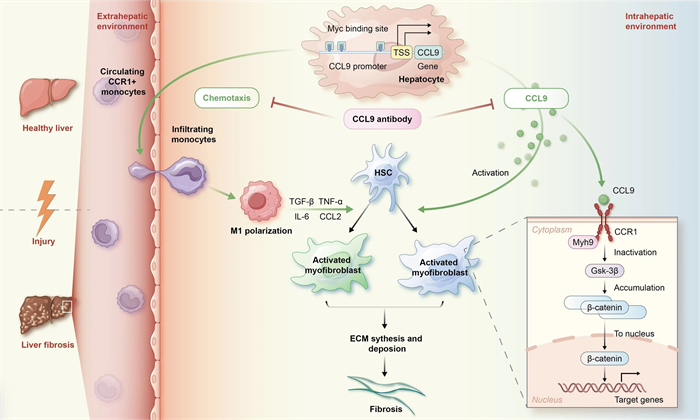
研究通过多种小鼠模型(包括四氯化碳诱导、胆管结扎和高脂蛋氨酸-胆碱缺乏饮食模型)系统探讨了Ccl9的功能。结果显示,在肝纤维化进程中,Ccl9在受损肝细胞中的表达显著上调,并受转录因子Myc的调控。进一步机制研究表明,Ccl9通过与其受体Ccr1结合,介导了肝脏微环境的炎症反应和纤维化进程。具体而言,Ccl9信号通路主要通过以下两种方式发挥作用:一是促进巨噬细胞向肝脏浸润并诱导其M1型极化,从而增强炎症因子(如TNF-α和IL-6)的释放,加剧肝脏炎症和损伤;二是直接激活肝星状细胞(HSCs),通过Ccr1招募Myh9蛋白,增强Wnt信号通路(通过Myh9介导的Gsk3β泛素化),从而加速HSCs的活化和胶原沉积。实验验证表明,肝细胞特异性敲除Ccl9或使用Ccl9中和抗体可显著缓解肝纤维化程度,表现为炎症反应减弱、巨噬细胞和中性粒细胞浸润减少、纤维化标志物(如α-SMA和Collagen I)表达下降。这些发现明确了Ccl9作为肝纤维化关键促纤维化因子的角色,为后续药物靶点开发奠定了实验基础。值得注意的是,人类同源分子Ccl15在肝癌患者中异常高表达,提示靶向该通路可能兼具抗纤维化与肝癌预防的双重潜力。
作为肝癌防治的关键环节,肝纤维化的可逆性为临床干预提供了重要窗口。李悦国团队的研究聚焦于Ccl9的作用,为肝纤维化与肝癌之间潜在联系的探索提供了新线索,Ccl9诱导的炎症微环境和HSCs活化可能与肝癌发生存在间接关联。例如,Ccl9促进的巨噬细胞M1极化和炎症反应可能加剧肝细胞的氧化应激和DNA损伤,而活化的HSCs可能在肝癌微环境中进一步演变为肿瘤相关成纤维细胞(CAFs),支持肿瘤的生长和侵袭。基于此,阻断Ccl9信号通路不仅有望缓解肝纤维化,还可能降低由纤维化驱动的癌变风险。天津医科大学肿瘤医院李悦国教授团队将继续关注肝纤维化与肝癌之间的病理联系,未来或将基于Ccl9的发现,进一步探索其在肝癌预防和治疗中的应用潜力。这一研究为肝病和肿瘤领域的交叉研究提供了宝贵基础,凸显了从肝纤维化入手干预肝癌的科学价值和临床意义。

通讯作者 李悦国
天津医科大学肿瘤医院
检验科副主任
临床PI
主任医师、博士生导师、博士后合作导师
天津市抗癌协会肿瘤转化医学专业委员会主任委员,天津医科大学医院“临床人才培养123攀登计划”第二层次人才。主要研究方向为肝癌及其相关肝病关键分子的基础及临床转化应用等。主持完成两项国家自然科学基金项目及多项省部级课题。以通讯作者在Hepatology, Drug resistance updates, ACS applied materials & interfaces, Biosensors & bioelectronics, Cancer letters等国际权威学术期刊发表SCI论文多篇。